Hukum dasar kimia adalah prinsip-prinsip dasar yang mendasari perilaku materi dan perubahannya. Hukum-hukum ini menjelaskan sifat atom, molekul, dan reaksi kimia, serta membantu kita memahami dunia di sekitar kita.
Hukum dasar kimia sangat penting karena memungkinkan kita untuk memprediksi dan mengendalikan reaksi kimia. Hal ini memiliki aplikasi luas dalam berbagai bidang, termasuk kedokteran, pertanian, dan manufaktur. Pemahaman tentang hukum dasar kimia juga penting untuk memahami isu-isu lingkungan, seperti polusi dan perubahan iklim.
Hukum dasar kimia telah berkembang selama berabad-abad, dimulai dengan karya para filsuf Yunani kuno. Pada abad ke-18, Antoine Lavoisier meletakkan dasar kimia modern dengan hukum kekekalan massa. Sejak itu, para ilmuwan telah terus membangun hukum-hukum ini, dan kita sekarang memiliki pemahaman yang komprehensif tentang cara kerja materi.
hukum dasar kimia
Hukum dasar kimia adalah prinsip-prinsip dasar yang mengatur perilaku materi dan perubahannya. Hukum-hukum ini sangat penting karena memungkinkan kita untuk memahami dan memprediksi reaksi kimia.
- Kekekalan massa
- Komposisi tetap
- Perbandingan berganda
- Volume gas
- Termodinamika
- Kesetimbangan kimia
- Laju reaksi
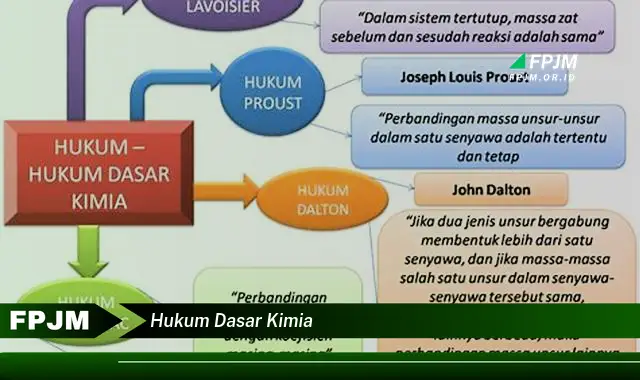
Hukum kekekalan massa menyatakan bahwa massa zat-zat dalam suatu reaksi kimia tetap sama. Hukum komposisi tetap menyatakan bahwa suatu senyawa kimia selalu memiliki komposisi unsur-unsur yang sama. Hukum perbandingan berganda menyatakan bahwa jika dua unsur membentuk lebih dari satu senyawa, maka perbandingan massa salah satu unsur yang bergabung dengan massa tetap unsur lainnya adalah bilangan bulat sederhana. Hukum volume gas menyatakan bahwa volume gas-gas yang bereaksi atau dihasilkan dalam suatu reaksi kimia berada dalam perbandingan bilangan bulat sederhana. Hukum termodinamika menyatakan bahwa entropi alam semesta selalu meningkat. Hukum kesetimbangan kimia menyatakan bahwa pada suatu saat tertentu, laju reaksi maju dan laju reaksi balik dalam suatu reaksi kimia adalah sama. Hukum laju reaksi menyatakan bahwa laju suatu reaksi kimia bergantung pada konsentrasi reaktan, suhu, dan katalis.
Kekekalan massa
Kekekalan massa adalah hukum dasar kimia yang menyatakan bahwa massa zat-zat dalam suatu reaksi kimia tetap sama. Hukum ini sangat penting karena memungkinkan kita untuk memahami dan memprediksi reaksi kimia.
-
Penerapan dalam kehidupan sehari-hari
Hukum kekekalan massa dapat diterapkan dalam kehidupan sehari-hari, misalnya saat kita memasak. Ketika kita merebus air, massa air akan tetap sama, meskipun air tersebut berubah menjadi uap. Hal ini karena uap air masih mengandung molekul air yang sama seperti saat masih berbentuk cair. -
Implikasi dalam kimia
Hukum kekekalan massa memiliki implikasi penting dalam kimia. Salah satunya adalah hukum ini dapat digunakan untuk menentukan massa reaktan dan produk dalam suatu reaksi kimia. Hukum ini juga dapat digunakan untuk menghitung perubahan entalpi reaksi. -
Contoh reaksi kimia
Contoh reaksi kimia yang menunjukkan hukum kekekalan massa adalah reaksi pembakaran metana. Dalam reaksi ini, metana bereaksi dengan oksigen menghasilkan karbon dioksida dan air. Massa total reaktan (metana dan oksigen) sama dengan massa total produk (karbon dioksida dan air). -
Hubungan dengan hukum dasar kimia lainnya
Hukum kekekalan massa terkait erat dengan hukum dasar kimia lainnya, seperti hukum komposisi tetap dan hukum perbandingan berganda. Hukum-hukum ini bersama-sama membentuk dasar pemahaman kita tentang reaksi kimia.
Dengan memahami hukum kekekalan massa, kita dapat lebih memahami dan memprediksi reaksi kimia. Hukum ini merupakan dasar penting untuk banyak aplikasi kimia, termasuk sintesis bahan kimia baru dan pengembangan teknologi baru.
Komposisi tetap
Hukum komposisi tetap menyatakan bahwa suatu senyawa kimia selalu memiliki komposisi unsur-unsur yang sama. Hukum ini sangat penting karena memungkinkan kita untuk memahami dan memprediksi sifat-sifat senyawa kimia.
Contohnya, air selalu terdiri dari dua atom hidrogen dan satu atom oksigen. Tidak peduli bagaimana kita membuat air, komposisinya akan selalu sama. Hal ini karena atom-atom dalam suatu senyawa kimia terikat bersama dalam perbandingan tetap.
Hukum komposisi tetap memiliki banyak aplikasi praktis. Misalnya, hukum ini dapat digunakan untuk menentukan rumus kimia suatu senyawa. Hukum ini juga dapat digunakan untuk menghitung massa reaktan dan produk dalam suatu reaksi kimia.
Memahami hukum komposisi tetap sangat penting untuk memahami kimia. Hukum ini merupakan dasar untuk banyak aplikasi kimia, termasuk sintesis bahan kimia baru dan pengembangan teknologi baru.
Perbandingan berganda
Hukum perbandingan berganda menyatakan bahwa jika dua unsur membentuk lebih dari satu senyawa, maka perbandingan massa salah satu unsur yang bergabung dengan massa tetap unsur lainnya adalah bilangan bulat sederhana. Hukum ini sangat penting karena memungkinkan kita untuk memahami dan memprediksi komposisi senyawa kimia.
Contohnya, karbon dan oksigen membentuk dua senyawa, yaitu karbon monoksida (CO) dan karbon dioksida (CO2). Dalam karbon monoksida, perbandingan massa karbon dengan massa oksigen adalah 12:16, sedangkan dalam karbon dioksida, perbandingan massa karbon dengan massa oksigen adalah 12:32. Kedua perbandingan ini adalah bilangan bulat sederhana, yaitu 1:1 dan 1:2.
Hukum perbandingan berganda memiliki banyak aplikasi praktis. Misalnya, hukum ini dapat digunakan untuk menentukan rumus kimia suatu senyawa. Hukum ini juga dapat digunakan untuk menghitung massa reaktan dan produk dalam suatu reaksi kimia.
Memahami hukum perbandingan berganda sangat penting untuk memahami kimia. Hukum ini merupakan dasar untuk banyak aplikasi kimia, termasuk sintesis bahan kimia baru dan pengembangan teknologi baru.
Volume gas
Hukum volume gas merupakan salah satu hukum dasar kimia yang menjelaskan hubungan antara volume gas dengan tekanan, suhu, dan jumlah mol gas. Hukum ini sangat penting karena memungkinkan kita untuk memahami dan memprediksi perilaku gas dalam berbagai kondisi.
Hukum volume gas memiliki beberapa bagian, yaitu:
- Hukum Boyle: Hukum ini menyatakan bahwa pada suhu tetap, volume gas berbanding terbalik dengan tekanannya. Artinya, jika tekanan gas diperbesar, maka volumenya akan mengecil, begitu pula sebaliknya.
- Hukum Charles: Hukum ini menyatakan bahwa pada tekanan tetap, volume gas berbanding lurus dengan suhunya. Artinya, jika suhu gas dinaikkan, maka volumenya akan membesar, begitu pula sebaliknya.
- Hukum Avogadro: Hukum ini menyatakan bahwa pada suhu dan tekanan yang sama, volume gas-gas yang berbeda berbanding lurus dengan jumlah mol gas tersebut. Artinya, jika jumlah mol gas diperbesar, maka volumenya akan membesar, begitu pula sebaliknya.
Hukum volume gas memiliki banyak aplikasi praktis, di antaranya:
- Perancangan balon udara: Balon udara dapat terbang karena diisi dengan gas yang lebih ringan dari udara. Hukum volume gas digunakan untuk menghitung volume gas yang dibutuhkan untuk mengangkat balon ke udara.
- Pengisian tabung gas: Tabung gas digunakan untuk menyimpan gas bertekanan tinggi. Hukum volume gas digunakan untuk menghitung jumlah gas yang dapat disimpan dalam tabung pada tekanan tertentu.
- Analisis gas: Hukum volume gas digunakan untuk menganalisis komposisi gas dengan membandingkan volumenya pada tekanan dan suhu yang berbeda.
Memahami hukum volume gas sangat penting untuk memahami kimia dan berbagai aplikasinya. Hukum ini merupakan dasar untuk banyak teknologi modern, seperti balon udara, tabung gas, dan analisis gas.
Termodinamika
Termodinamika adalah cabang ilmu kimia yang mempelajari energi dan perubahannya. Termodinamika berperan penting dalam hukum dasar kimia karena membantu kita memahami bagaimana reaksi kimia berlangsung dan bagaimana energi terlibat dalam reaksi tersebut.
-
Energi dalam reaksi kimia
Termodinamika membantu kita memahami bagaimana energi dilepaskan atau diserap dalam reaksi kimia. Reaksi eksotermik melepaskan energi, sedangkan reaksi endotermik menyerap energi. Pengetahuan tentang energi reaksi sangat penting untuk merancang dan mengendalikan reaksi kimia.
-
Entropi dan spontanitas reaksi
Termodinamika juga membantu kita memahami konsep entropi dan spontanitas reaksi. Entropi adalah ukuran ketidakteraturan suatu sistem. Reaksi spontan adalah reaksi yang berlangsung dengan peningkatan entropi. Pengetahuan tentang entropi sangat penting untuk memprediksi arah reaksi kimia.
-
Kesetimbangan kimia
Termodinamika juga berperan dalam memahami kesetimbangan kimia. Kesetimbangan kimia adalah keadaan ketika laju reaksi maju dan laju reaksi balik sama. Termodinamika membantu kita memahami faktor-faktor yang mempengaruhi kesetimbangan kimia dan bagaimana cara menggeser kesetimbangan ke arah yang diinginkan.
-
Aplikasi dalam kehidupan sehari-hari
Termodinamika memiliki banyak aplikasi dalam kehidupan sehari-hari, seperti dalam pengembangan mesin, refrigerasi, dan pemanasan. Pengetahuan tentang termodinamika sangat penting untuk memahami dan merancang sistem yang melibatkan perubahan energi.
Dengan memahami termodinamika, kita dapat lebih memahami dan memprediksi reaksi kimia. Termodinamika merupakan dasar penting untuk banyak aplikasi kimia, termasuk sintesis bahan kimia baru, pengembangan teknologi baru, dan pemahaman proses alam.
Kesetimbangan kimia
Kesetimbangan kimia merupakan salah satu konsep dasar dalam kimia yang menjelaskan tentang keadaan keseimbangan suatu reaksi kimia, di mana laju reaksi maju dan laju reaksi balik sama. Konsep ini sangat penting karena membantu kita memahami berbagai aspek perilaku reaksi kimia.
-
Posisi kesetimbangan
Posisi kesetimbangan suatu reaksi kimia dipengaruhi oleh beberapa faktor, seperti konsentrasi reaktan dan produk, suhu, dan tekanan. Memahami faktor-faktor ini memungkinkan kita mengontrol dan menggeser posisi kesetimbangan ke arah yang diinginkan. -
Aplikasi dalam industri
Konsep kesetimbangan kimia banyak digunakan dalam industri, misalnya pada proses produksi amonia (NH3) dan asam sulfat (H2SO4). Dengan mengendalikan kondisi reaksi, seperti suhu dan tekanan, industri dapat mengoptimalkan hasil produksi. -
Kesetimbangan dalam sistem biologis
Kesetimbangan kimia juga memainkan peran penting dalam sistem biologis. Misalnya, kesetimbangan antara karbon dioksida (CO2) dan air (H2O) dalam darah sangat penting untuk mengatur pH darah dan pernapasan.
Dengan memahami konsep kesetimbangan kimia, kita dapat lebih memahami dan mengendalikan berbagai reaksi kimia. Konsep ini merupakan dasar penting untuk banyak aplikasi kimia, termasuk sintesis bahan kimia baru, pengembangan teknologi baru, dan pemahaman proses alam.
Laju reaksi
Laju reaksi merupakan besaran yang menyatakan perubahan konsentrasi reaktan atau produk tiap satuan waktu. Laju reaksi sangat penting dalam hukum dasar kimia karena dapat digunakan untuk memprediksi laju suatu reaksi dan menentukan faktor-faktor yang mempengaruhinya.
Salah satu hukum dasar kimia yang berkaitan dengan laju reaksi adalah hukum laju reaksi. Hukum laju reaksi menyatakan bahwa laju suatu reaksi bergantung pada konsentrasi reaktan, suhu, dan katalis. Dengan memahami hukum laju reaksi, kita dapat mengontrol dan mengoptimalkan laju reaksi dalam berbagai aplikasi kimia.
Contoh penerapan hukum dasar kimia dalam kehidupan sehari-hari adalah pada proses pembakaran. Laju pembakaran dapat dipengaruhi oleh faktor-faktor seperti jenis bahan bakar, konsentrasi oksigen, dan suhu. Pemahaman tentang hukum dasar kimia memungkinkan kita untuk mengendalikan laju pembakaran dan mencegah terjadinya kebakaran yang tidak diinginkan.
Selain itu, hukum dasar kimia juga penting dalam industri kimia. Dalam industri makanan, misalnya, hukum dasar kimia digunakan untuk mengontrol laju reaksi fermentasi dan pasteurisasi. Dalam industri farmasi, hukum dasar kimia digunakan untuk mengoptimalkan laju produksi obat-obatan.
Dengan memahami hukum dasar kimia, khususnya laju reaksi, kita dapat mengendalikan dan mengoptimalkan berbagai proses kimia. Pemahaman ini sangat penting untuk pengembangan teknologi baru dan peningkatan efisiensi proses industri.
Pertanyaan Umum tentang Hukum Dasar Kimia
Hukum dasar kimia adalah prinsip-prinsip dasar yang mengatur perilaku materi dan perubahannya. Hukum-hukum ini sangat penting untuk memahami dan memprediksi reaksi kimia. Berikut adalah beberapa pertanyaan umum tentang hukum dasar kimia:
Pertanyaan 1: Apa saja hukum dasar kimia yang paling penting?
Beberapa hukum dasar kimia yang paling penting antara lain:
- Hukum kekekalan massa
- Hukum komposisi tetap
- Hukum perbandingan berganda
- Hukum volume gas
- Hukum termodinamika
- Hukum kesetimbangan kimia
- Hukum laju reaksi
Pertanyaan 2: Bagaimana hukum dasar kimia digunakan dalam kehidupan sehari-hari?
Hukum dasar kimia digunakan dalam kehidupan sehari-hari dalam berbagai cara, misalnya:
- Saat kita memasak, hukum kekekalan massa membantu kita memahami bahwa massa total bahan-bahan yang kita gunakan akan sama dengan massa total makanan yang dihasilkan.
- Saat kita mengembang ban mobil, hukum volume gas membantu kita memahami bahwa volume udara di dalam ban akan meningkat seiring bertambahnya tekanan.
- Saat kita menggunakan obat-obatan, hukum laju reaksi membantu kita memahami bagaimana tubuh kita akan menyerap dan memetabolisme obat tersebut.
Pertanyaan 3: Bagaimana hukum dasar kimia digunakan dalam industri?
Hukum dasar kimia digunakan dalam industri dalam berbagai cara, misalnya:
- Dalam industri makanan, hukum dasar kimia digunakan untuk mengontrol laju reaksi fermentasi dan pasteurisasi.
- Dalam industri farmasi, hukum dasar kimia digunakan untuk mengoptimalkan laju produksi obat-obatan.
- Dalam industri kimia, hukum dasar kimia digunakan untuk mengembangkan bahan-bahan baru dan meningkatkan efisiensi proses produksi.
Pertanyaan 4: Mengapa hukum dasar kimia penting untuk dipelajari?
Hukum dasar kimia penting untuk dipelajari karena:
- Hukum-hukum ini membantu kita memahami cara kerja materi dan perubahannya.
- Hukum-hukum ini dapat digunakan untuk memprediksi dan mengendalikan reaksi kimia.
- Hukum-hukum ini sangat penting untuk berbagai aplikasi di bidang sains, teknik, dan industri.
Dengan memahami hukum dasar kimia, kita dapat lebih memahami dunia di sekitar kita dan mengembangkan teknologi baru untuk meningkatkan kehidupan kita.
Ringkasan
Hukum dasar kimia adalah prinsip-prinsip dasar yang mengatur perilaku materi dan perubahannya. Hukum-hukum ini sangat penting untuk memahami dan memprediksi reaksi kimia, serta memiliki berbagai aplikasi dalam kehidupan sehari-hari, industri, dan sains.
Transisi ke Bagian Tips
Untuk mempelajari lebih lanjut tentang hukum dasar kimia, berikut beberapa tips:
Tips Mempelajari Hukum Dasar Kimia
Hukum dasar kimia merupakan prinsip-prinsip dasar yang mengatur perilaku materi dan perubahannya. Hukum-hukum ini sangat penting untuk dipahami dan dikuasai dalam mempelajari kimia. Berikut adalah beberapa tips untuk mempelajari hukum dasar kimia:
Tip 1: Pahami Konsep Dasar
Sebelum mempelajari hukum dasar kimia, pastikan Anda memahami konsep dasar kimia, seperti struktur atom, ikatan kimia, dan reaksi kimia. Konsep-konsep ini akan menjadi dasar untuk memahami hukum dasar kimia.
Tip 2: Pelajari Hukum Secara Teratur
Hukum dasar kimia terdiri dari beberapa hukum, seperti hukum kekekalan massa, hukum komposisi tetap, dan hukum volume gas. Pelajarilah hukum-hukum ini secara teratur dan bertahap. Jangan mencoba menghafal semua hukum sekaligus, tetapi fokuslah pada memahami konsep di balik setiap hukum.
Tip 3: Latihan Soal
Untuk menguji pemahaman Anda tentang hukum dasar kimia, kerjakanlah latihan soal sebanyak mungkin. Latihan soal akan membantu Anda mengidentifikasi kelemahan Anda dan meningkatkan pemahaman Anda tentang hukum-hukum tersebut.
Tip 4: Aplikasi dalam Kehidupan Nyata
Untuk membuat pembelajaran lebih menarik, cobalah untuk mengaitkan hukum dasar kimia dengan kehidupan nyata. Misalnya, Anda dapat menggunakan hukum kekekalan massa untuk memahami mengapa massa suatu benda tidak berubah setelah reaksi kimia.
Dengan mengikuti tips-tips ini, Anda dapat mempelajari hukum dasar kimia dengan lebih efektif dan mendalam. Pemahaman yang baik tentang hukum-hukum ini akan membantu Anda dalam mempelajari kimia lebih lanjut dan menerapkannya dalam berbagai bidang.
Kesimpulan
Hukum dasar kimia sangat penting untuk dipahami dalam mempelajari kimia. Dengan memahami hukum-hukum ini, Anda dapat memprediksi dan mengendalikan reaksi kimia, serta mengembangkan teknologi baru untuk meningkatkan kehidupan kita.
Kesimpulan
Hukum dasar kimia merupakan prinsip dasar yang mengatur perilaku materi dan perubahannya. Hukum-hukum ini sangat penting untuk memahami dan memprediksi reaksi kimia, serta memiliki berbagai aplikasi dalam kehidupan sehari-hari, industri, dan sains.
Dengan memahami hukum dasar kimia, kita dapat lebih memahami dunia di sekitar kita dan mengembangkan teknologi baru untuk meningkatkan kehidupan kita. Oleh karena itu, mempelajari dan memahami hukum dasar kimia sangat penting bagi siapa saja yang ingin berkecimpung dalam bidang sains dan teknologi.




