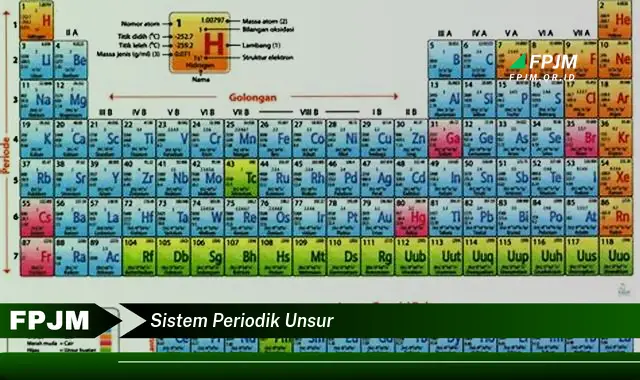
Sistem periodik unsur adalah tabel yang menyusun unsur-unsur kimia berdasarkan nomor atom, konfigurasi elektron, dan sifat kimia yang berulang. Tabel ini pertama kali dikembangkan oleh Dmitri Mendeleev pada tahun 1869.
Sistem periodik unsur sangat penting karena memungkinkan para ilmuwan untuk memprediksi sifat suatu unsur berdasarkan posisinya dalam tabel. Sistem ini juga membantu para ilmuwan untuk memahami hubungan antara struktur atom dan sifat kimia.
Sistem periodik unsur memiliki banyak kegunaan dalam bidang kimia, fisika, dan biologi. Sistem ini digunakan untuk mengklasifikasikan unsur, memprediksi reaktivitas, dan merancang bahan baru.
Sistem Periodik Unsur
Sistem periodik unsur sangat penting untuk memahami sifat dan perilaku unsur-unsur kimia. Sistem ini memiliki beberapa aspek penting, yaitu:
- Unsur
- Nomor atom
- Konfigurasi elektron
- Periode
- Golongan
- Sifat kimia
- Reaktivitas
Aspek-aspek ini saling berkaitan dan menentukan sifat unsur-unsur kimia. Misalnya, nomor atom suatu unsur menentukan jumlah proton dalam nukleusnya, yang pada gilirannya menentukan jumlah elektron dalam kulit atomnya. Konfigurasi elektron suatu unsur menentukan sifat kimianya, seperti reaktivitas dan kemampuannya untuk membentuk ikatan dengan unsur lain. Posisi suatu unsur dalam sistem periodik juga dapat digunakan untuk memprediksi sifat-sifatnya. Misalnya, unsur-unsur yang berada dalam golongan yang sama biasanya memiliki sifat kimia yang mirip.
Unsur
Unsur adalah zat kimia murni yang tidak dapat dibagi lagi menjadi zat yang lebih sederhana melalui reaksi kimia biasa. Unsur-unsur merupakan penyusun dasar segala materi di alam semesta.
Sistem periodik unsur adalah sebuah tabel yang menyusun unsur-unsur berdasarkan nomor atom, konfigurasi elektron, dan sifat kimia yang berulang. Sistem ini pertama kali dikembangkan oleh Dmitri Mendeleev pada tahun 1869.
Unsur-unsur merupakan komponen dasar dari sistem periodik unsur. Setiap unsur memiliki sifat kimia yang unik yang ditentukan oleh jumlah proton dalam nukleusnya. Sifat-sifat ini menentukan bagaimana unsur-unsur berinteraksi satu sama lain dan membentuk senyawa.
Sistem periodik unsur sangat penting untuk memahami sifat dan perilaku unsur-unsur kimia. Sistem ini digunakan oleh para ilmuwan untuk memprediksi sifat suatu unsur berdasarkan posisinya dalam tabel. Sistem ini juga membantu para ilmuwan untuk memahami hubungan antara struktur atom dan sifat kimia.
Nomor Atom
Nomor atom adalah jumlah proton dalam inti atom suatu unsur. Nomor atom menentukan identitas unsur dan posisinya dalam sistem periodik unsur.
Dalam sistem periodik unsur, unsur-unsur disusun berdasarkan nomor atomnya, dari yang terkecil hingga yang terbesar. Unsur-unsur yang memiliki nomor atom yang sama berada dalam golongan yang sama, dan unsur-unsur yang berada dalam periode yang sama memiliki jumlah kulit elektron yang sama.
Nomor atom sangat penting dalam sistem periodik unsur karena menentukan sifat kimia suatu unsur. Unsur-unsur yang berada dalam golongan yang sama memiliki sifat kimia yang mirip karena memiliki jumlah elektron valensi yang sama. Elektron valensi adalah elektron pada kulit terluar atom, dan elektron inilah yang terlibat dalam reaksi kimia.
Memahami hubungan antara nomor atom dan sistem periodik unsur sangat penting untuk memahami sifat dan perilaku unsur-unsur kimia. Pengetahuan ini memiliki aplikasi yang luas dalam bidang kimia, fisika, dan biologi.
Konfigurasi Elektron
Konfigurasi elektron adalah susunan elektron-elektron dalam kulit-kulit atom suatu unsur. Konfigurasi elektron sangat penting dalam sistem periodik unsur karena menentukan sifat kimia suatu unsur.
-
Sifat Kimia
Sifat kimia suatu unsur ditentukan oleh elektron-elektron pada kulit terluarnya, yang disebut elektron valensi. Elektron valensi terlibat dalam pembentukan ikatan kimia dengan unsur lain. Unsur-unsur yang memiliki jumlah elektron valensi yang sama memiliki sifat kimia yang mirip. Misalnya, unsur-unsur golongan 1A (logam alkali) memiliki satu elektron valensi dan sangat reaktif.
-
Posisi dalam Sistem Periodik Unsur
Konfigurasi elektron juga menentukan posisi suatu unsur dalam sistem periodik unsur. Unsur-unsur yang memiliki jumlah elektron valensi yang sama berada dalam golongan yang sama. Unsur-unsur yang berada dalam periode yang sama memiliki jumlah kulit elektron yang sama.
-
Ikatan Kimia
Konfigurasi elektron suatu unsur menentukan jenis ikatan kimia yang dapat dibentuknya. Misalnya, unsur-unsur golongan 1A cenderung membentuk ikatan ionik, sedangkan unsur-unsur golongan 7A (halogen) cenderung membentuk ikatan kovalen.
-
Prediksi Sifat Unsur
Konfigurasi elektron suatu unsur dapat digunakan untuk memprediksi sifat-sifatnya, seperti titik leleh, titik didih, dan kerapatan. Hal ini karena konfigurasi elektron menentukan ukuran dan bentuk atom, yang pada gilirannya menentukan sifat fisik dan kimia suatu unsur.
Memahami hubungan antara konfigurasi elektron dan sistem periodik unsur sangat penting untuk memahami sifat dan perilaku unsur-unsur kimia. Pengetahuan ini memiliki aplikasi yang luas dalam bidang kimia, fisika, dan biologi.
Periode
Periode dalam sistem periodik unsur adalah deretan horizontal yang menyusun unsur-unsur berdasarkan jumlah kulit elektronnya. Periode menentukan sifat kimia dan fisik unsur-unsur.
Unsur-unsur dalam periode yang sama memiliki jumlah kulit elektron yang sama. Hal ini berarti bahwa unsur-unsur dalam periode yang sama memiliki sifat kimia yang mirip. Misalnya, semua unsur dalam periode 2 adalah gas pada suhu kamar.
Periode sangat penting dalam sistem periodik unsur karena memungkinkan para ilmuwan untuk memprediksi sifat suatu unsur berdasarkan posisinya dalam tabel. Misalnya, jika seorang ilmuwan mengetahui bahwa suatu unsur berada pada periode 3, maka mereka dapat memprediksi bahwa unsur tersebut memiliki tiga kulit elektron dan kemungkinan besar berwujud padat pada suhu kamar.
Memahami hubungan antara periode dan sistem periodik unsur sangat penting untuk memahami sifat dan perilaku unsur-unsur kimia. Pengetahuan ini memiliki aplikasi yang luas dalam bidang kimia, fisika, dan biologi.
Golongan
Golongan dalam sistem periodik unsur adalah kolom vertikal yang menyusun unsur-unsur berdasarkan jumlah elektron valensinya. Golongan sangat penting dalam sistem periodik unsur karena menentukan sifat kimia suatu unsur.
-
Sifat Kimia
Sifat kimia suatu unsur ditentukan oleh elektron-elektron pada kulit terluarnya, yang disebut elektron valensi. Golongan mengelompokkan unsur-unsur yang memiliki jumlah elektron valensi yang sama, sehingga unsur-unsur dalam golongan yang sama memiliki sifat kimia yang mirip. Misalnya, unsur-unsur golongan 1A (logam alkali) memiliki satu elektron valensi dan sangat reaktif.
-
Reaktivitas
Reaktivitas suatu unsur juga dipengaruhi oleh jumlah elektron valensinya. Unsur-unsur yang memiliki sedikit elektron valensi cenderung lebih reaktif daripada unsur-unsur yang memiliki banyak elektron valensi. Misalnya, unsur-unsur golongan 1A (logam alkali) sangat reaktif karena hanya memiliki satu elektron valensi.
-
Ikatan Kimia
Jumlah elektron valensi juga menentukan jenis ikatan kimia yang dapat dibentuk oleh suatu unsur. Misalnya, unsur-unsur golongan 1A (logam alkali) cenderung membentuk ikatan ionik, sedangkan unsur-unsur golongan 7A (halogen) cenderung membentuk ikatan kovalen.
-
Prediksi Sifat Unsur
Golongan dapat digunakan untuk memprediksi sifat-sifat suatu unsur, seperti titik leleh, titik didih, dan kerapatan. Hal ini karena golongan menentukan jumlah elektron valensi suatu unsur, yang pada gilirannya menentukan sifat fisik dan kimianya.
Memahami hubungan antara golongan dan sistem periodik unsur sangat penting untuk memahami sifat dan perilaku unsur-unsur kimia. Pengetahuan ini memiliki aplikasi yang luas dalam bidang kimia, fisika, dan biologi.
Sifat Kimia
Sifat kimia merupakan salah satu aspek penting dalam sistem periodik unsur. Sifat kimia suatu unsur menentukan bagaimana unsur tersebut bereaksi dengan unsur lain untuk membentuk senyawa.
-
Posisi dalam Sistem Periodik Unsur
Posisi suatu unsur dalam sistem periodik unsur dapat digunakan untuk memprediksi sifat kimianya. Unsur-unsur yang berada dalam golongan yang sama memiliki sifat kimia yang mirip karena memiliki jumlah elektron valensi yang sama. Misalnya, unsur-unsur golongan 1A (logam alkali) sangat reaktif karena memiliki satu elektron valensi.
-
Elektron Valensi
Jumlah elektron valensi suatu unsur menentukan sifat kimianya. Elektron valensi adalah elektron pada kulit terluar atom, dan elektron inilah yang terlibat dalam reaksi kimia. Unsur-unsur yang memiliki sedikit elektron valensi cenderung lebih reaktif daripada unsur-unsur yang memiliki banyak elektron valensi.
-
Ikatan Kimia
Sifat kimia suatu unsur juga menentukan jenis ikatan kimia yang dapat dibentuknya. Misalnya, unsur-unsur golongan 1A (logam alkali) cenderung membentuk ikatan ionik, sedangkan unsur-unsur golongan 7A (halogen) cenderung membentuk ikatan kovalen.
-
Reaktivitas
Reaktivitas suatu unsur bergantung pada sifat kimianya. Unsur-unsur yang memiliki sifat kimia yang reaktif cenderung mudah bereaksi dengan unsur lain. Misalnya, unsur-unsur golongan 1A (logam alkali) sangat reaktif karena memiliki sedikit elektron valensi.
Dengan memahami sifat kimia suatu unsur dan hubungannya dengan sistem periodik unsur, para ilmuwan dapat memprediksi reaksi kimia yang akan terjadi dan merancang bahan-bahan baru dengan sifat yang diinginkan.
Reaktivitas
Reaktivitas adalah kecenderungan suatu unsur untuk bereaksi dengan unsur lain membentuk senyawa baru. Reaktivitas unsur sangat dipengaruhi oleh posisi unsur dalam sistem periodik unsur.
-
Posisi dalam Golongan
Unsur-unsur yang terletak dalam satu golongan memiliki jumlah elektron valensi yang sama. Jumlah elektron valensi ini sangat menentukan reaktivitas suatu unsur. Unsur-unsur dengan sedikit elektron valensi cenderung lebih reaktif dibandingkan unsur-unsur dengan banyak elektron valensi. Misalnya, logam alkali (golongan IA) memiliki satu elektron valensi dan merupakan unsur-unsur yang sangat reaktif, sedangkan gas mulia (golongan VIIIA) memiliki delapan elektron valensi dan merupakan unsur-unsur yang tidak reaktif.
-
Posisi dalam Periode
Unsur-unsur yang terletak dalam satu periode memiliki jumlah kulit elektron yang sama. Semakin ke kanan suatu periode, jari-jari atom semakin kecil dan gaya tarik inti terhadap elektron valensi semakin besar. Hal ini menyebabkan unsur-unsur di sebelah kanan suatu periode cenderung kurang reaktif dibandingkan unsur-unsur di sebelah kirinya. Misalnya, dalam periode 2, fluor (F) lebih reaktif dibandingkan oksigen (O), dan oksigen lebih reaktif dibandingkan nitrogen (N).
-
Konfigurasi Elektron
Konfigurasi elektron suatu unsur juga dapat mempengaruhi reaktivitasnya. Unsur-unsur dengan elektron valensi yang tidak berpasangan cenderung lebih reaktif dibandingkan unsur-unsur dengan elektron valensi yang berpasangan. Misalnya, oksigen (O) memiliki dua elektron valensi yang tidak berpasangan dan merupakan unsur yang sangat reaktif, sedangkan neon (Ne) memiliki delapan elektron valensi yang berpasangan dan merupakan unsur yang tidak reaktif.
-
Sifat Logam dan Nonlogam
Unsur-unsur logam cenderung lebih reaktif dibandingkan unsur-unsur nonlogam. Hal ini disebabkan karena unsur-unsur logam memiliki energi ionisasi yang rendah dan mudah melepaskan elektron valensinya. Sedangkan unsur-unsur nonlogam cenderung lebih kurang reaktif dibandingkan unsur-unsur logam karena memiliki energi ionisasi yang tinggi dan sulit melepaskan elektron valensinya.
Dengan memahami reaktivitas unsur-unsur dan hubungannya dengan sistem periodik unsur, para ilmuwan dapat memprediksi reaksi kimia yang akan terjadi, merancang bahan-bahan baru dengan sifat yang diinginkan, dan memahami berbagai fenomena alam yang melibatkan reaksi kimia.
Pertanyaan Umum tentang Sistem Periodik Unsur
Sistem periodik unsur adalah tabel yang menyusun unsur-unsur kimia berdasarkan nomor atom, konfigurasi elektron, dan sifat kimia yang berulang. Tabel ini pertama kali dikembangkan oleh Dmitri Mendeleev pada tahun 1869. Sistem periodik unsur sangat penting untuk memahami sifat dan perilaku unsur-unsur kimia. Berikut adalah beberapa pertanyaan umum tentang sistem periodik unsur:
Pertanyaan 1: Apa itu sistem periodik unsur?
Jawaban: Sistem periodik unsur adalah tabel yang menyusun unsur-unsur kimia berdasarkan nomor atom, konfigurasi elektron, dan sifat kimia yang berulang.
Pertanyaan 2: Mengapa sistem periodik unsur penting?
Jawaban: Sistem periodik unsur penting karena memungkinkan para ilmuwan untuk memprediksi sifat suatu unsur berdasarkan posisinya dalam tabel. Sistem ini juga membantu para ilmuwan untuk memahami hubungan antara struktur atom dan sifat kimia.
Pertanyaan 3: Bagaimana cara menggunakan sistem periodik unsur?
Jawaban: Sistem periodik unsur dapat digunakan untuk menemukan informasi tentang unsur-unsur kimia, seperti nomor atom, massa atom, konfigurasi elektron, dan sifat kimia. Sistem ini juga dapat digunakan untuk memprediksi reaktivitas dan membentuk ikatan kimia antar unsur.
Pertanyaan 4: Apa saja kegunaan sistem periodik unsur?
Jawaban: Sistem periodik unsur memiliki banyak kegunaan dalam bidang kimia, fisika, dan biologi. Sistem ini digunakan untuk mengklasifikasikan unsur, memprediksi reaktivitas, merancang bahan baru, dan memahami berbagai fenomena alam yang melibatkan reaksi kimia.
Kesimpulan
Sistem periodik unsur adalah alat penting untuk memahami sifat dan perilaku unsur-unsur kimia. Sistem ini memiliki banyak kegunaan dalam berbagai bidang ilmiah. Dengan memahami sistem periodik unsur, para ilmuwan dapat memprediksi reaksi kimia, merancang bahan baru, dan memahami dunia di sekitar kita.
Tips Memahami Sistem Periodik Unsur
Sistem periodik unsur merupakan tabel yang menyusun unsur-unsur kimia berdasarkan nomor atom, konfigurasi elektron, dan sifat kimia yang berulang. Memahami sistem periodik unsur sangat penting untuk mempelajari kimia dan bidang terkait lainnya.
Tip 1: Pahami Konsep Dasar
Sebelum mempelajari sistem periodik unsur, penting untuk memahami konsep dasar seperti nomor atom, massa atom, dan elektron valensi. Konsep-konsep ini akan membantu Anda memahami organisasi dan sifat unsur-unsur dalam sistem periodik unsur.
Tip 2: Pelajari Golongan dan Periode
Sistem periodik unsur dibagi menjadi golongan (kolom vertikal) dan periode (baris horizontal). Golongan menunjukkan jumlah elektron valensi, yang menentukan sifat kimia unsur, sedangkan periode menunjukkan jumlah kulit elektron. Memahami golongan dan periode akan membantu Anda memprediksi sifat unsur dan tren periodik.
Tip 3: Gunakan Sumber Daya yang Tersedia
Ada banyak sumber daya yang tersedia untuk membantu Anda mempelajari sistem periodik unsur, seperti tabel periodik interaktif, video penjelasan, dan buku teks. Manfaatkan sumber daya ini untuk memperkuat pemahaman Anda dan mempraktikkan identifikasi dan klasifikasi unsur.
Tip 4: Praktik dan Aplikasi
Pemahaman yang baik tentang sistem periodik unsur membutuhkan latihan dan aplikasi. Cobalah untuk memprediksi sifat unsur berdasarkan posisinya dalam tabel, memecahkan masalah yang melibatkan tren periodik, dan menggunakan sistem periodik unsur untuk menjelaskan berbagai fenomena kimia.
Dengan mengikuti tips ini, Anda dapat meningkatkan pemahaman Anda tentang sistem periodik unsur dan menggunakannya secara efektif dalam studi dan penelitian Anda.
Kesimpulan
Sistem periodik unsur merupakan representasi terorganisir dari unsur-unsur kimia yang menyediakan wawasan mendalam tentang sifat dan perilakunya. Sistem ini telah membentuk dasar pemahaman kita tentang kimia dan telah menjadi alat yang tak ternilai bagi para ilmuwan, insinyur, dan peneliti di seluruh dunia.
Melalui studi sistem periodik unsur, kita dapat mengidentifikasi tren periodik, memprediksi reaktivitas unsur, dan menjelaskan berbagai fenomena kimia. Sistem ini telah merevolusi cara kita mengklasifikasikan dan memahami materi, yang mengarah pada penemuan unsur-unsur baru, pengembangan bahan-bahan inovatif, dan kemajuan pesat dalam berbagai bidang ilmiah.
Dengan terus mengeksplorasi dan memahami sistem periodik unsur, kita membuka jalan bagi penemuan dan inovasi lebih lanjut, yang pada akhirnya akan membentuk masa depan sains dan teknologi.




